
TABELLE 7-1: Frühe Reports über Impfung-assoziierte Poliomyelitis, erschienen vor 1970.
Unerwünschte Vorkommnisse bei Kinder-Impfstoffen
Nachweis von Ursächlichkeit
Institute of Medicine (US)
Vaccine Safety Committee;
Stratton KR, Howe CJ, Johnston RB Jr., editors.
Washington (DC): National Academies Press (US); 1994.
Inhaltsverzeichnis
(Übersetzungen weiterer Kapitel)
1 Hintergrund und Geschichte
Poliomyelitis ist eine akute Infektionskrankheit, die durch ein Enterovirus verursacht wird. Es gibt drei Arten dieses Virus: Typen 1, 2 und 3. Jeder Typ ist fähig, Menschen zu infizieren; Es gibt keine Kreuz-Immunität und nur diejenigen Personen immun gegen jeden der drei Arten sind gegen alle drei Arten geschützt. Das Virus tritt durch den oralen oder respiratorischen Weg in den Körper ein und vermehrt sich im Rachen und Dünndarm. Innerhalb von 24 Stunden dringt es in die regionalen Lymphknoten ein, und nach weiteren 24 bis 48 Stunden tritt er in den Blutkreislauf ein, der ihn zu den sekundären Replikationsorten in vielen Organen führt und somit entwickelt sich Viremie, wird aufrechterhalten und verstärkt. Während der Periode der Viremie kann das Virus das zentrale Nervensystem erreichen und dort eine Infektion einleiten. Antikörper erscheinen innerhalb von 1 Woche bis 10 Tage nach der ersten Infektion, und Viremie hört dann auf, wahrscheinlich als Folge der Neutralisation durch die Antikörper. Nur 1 bis 2 Prozent der infizierten Personen entwickeln eine Erkrankung im Zentralnervensystem und noch weniger haben eine Restlähmung. Dennoch ist die Belastung dieser seltenen Konsequenzen groß, weil sie zum Tod oder zur lebenslangen Behinderung führt.
Obwohl es derzeit wirksame Impfstoffe gegen Poliovirus gibt, demonstrierten Hammon et al. (1953) noch bevor sie verfügbar wurden, die Wirksamkeit der passiven Immunisierung durch Injektionen von gepooltem Gamma-Globulin. Verschiedene Versuche zur Entwicklung eines Impfstoffs wurden durch das Fehlen eines wirksamen In-vitro-Systems der Virusreplikation vereitelt. Die Etablierung im Jahr 1949 der Gewebekultur-Technik zur Unterstützung des Viruswachstums machte die Entwicklung eines Impfstoffs möglich (Enders et al., 1949). Es war für diese Erkenntnisse, dass J.F. Enders, F.C. Robbins und T.H. Weller den Nobelpreis 1954 erhielten. Auf diese Entwicklung folgten Bemühungen, ausreichende Mengen des Virus zu erzeugen, um es zu inaktivieren und als Inertantigen zu verwenden. Ein alternativer Ansatz war, das Wildtyp-Virus abzuschwächen und es als replizierendes Antigen sicher zu machen. Beide Ansätze waren erfolgreich und heute gibt es zwei Formen des Impfstoffs:
IPV wurde 1953 von Jonas Salk (Salk, 1953, Salk et al., 1953) entwickelt; OPV wurde von Koprowski und Kollegen (1952) entwickelt, die die ersten waren, und Albert Sabin (1956). Eine erhöht potente IPV wurde in den späten 1970er Jahren entwickelt und wird heute verwendet. Derzeit sind IPV und die Sabin-Stämme von OPV für den Einsatz in den Vereinigten Staaten verfügbar; Allerdings ist OPV der Impfstoff für den allgemeinen Gebrauch empfohlen und ist die am häufigsten vorkommende (American Academy of Pediatrics, Ausschuss für Infektionskrankheiten, 1991).
Kurz nach der Zulassung von IPV im Jahr 1955 wurde festgestellt, dass der Impfstoff, der von Cutter hergestellt wurde, eine paralytische Erkrankung verursachte. Es enthielt restliches infektiöses Virus. Der Grund wurde auf die Methode der Inaktivierung zurückgeführt. Zu diesem Zeitpunkt war die Dynamik des Inaktivierungsprozesses nicht vollständig verstanden, und die Anforderungen der US-Regierung an die Impfstoffproduktion waren nicht eindeutig. Alle diese Probleme wurden seither korrigiert
Das erste OPV wurde 1960 nach einem umfangreichen Prozeß in der ehemaligen Sowjetunion (Benison, 1982) lizenziert. Bis dahin hatten über 100 Millionen Menschen in den ehemaligen Sowjetunion und Ostblockländern - außer Polen - den Sabin-Impfstoff erhalten (LaForce, 1990). Versuche von OPV in den Vereinigten Staaten folgten, und monovalente OPVs wurden schnell lizenziert. Das trivalente OPV, das heute verwendet wird, wurde 1963 lizenziert. In den 1962er Empfehlungen des US Public Health Service wurde keine Präferenz für die eine oder andere Form des Impfstoffs ausgedrückt (US Public Health Service, 1962), aber 1964 der Ausschuss für Infektiöse Krankheiten der American Academy of Pediatrics empfahlen die Verwendung von OPV.
Polio wurde als eine endemische Krankheit in den Vereinigten Staaten und vielen Entwicklungsländern beseitigt. Ausbrüche sind gelegentlich in Teilmengen von nicht geimpften anfälligen Personen aufgetreten. Eine anhaltende Besorgnis war die Möglichkeit der seltenen Komplikation der paralytischen Poliomyelitis bei Geimpften und Personen im Kontakt mit ihnen, insbesondere solchen mit beeinträchtigter Immunität. Dies wird später in diesem Kapitel ausführlich besprochen. Einige Länder, zum Beispiel Dänemark, verwenden einen gemischten Zeitplan von IPV, gefolgt von OPV. Andere Nationen, wie Finnland und Holland, setzen weiterhin auf IPV. Die Debatte über die relative Wirksamkeit von OPV gegenüber der IPV setzt sich in der Literatur fort, ebenso wie die Debatte über die Verwendung von kombinierten Zeitplänen von IPV und OPV (Institute od Medicine, 1977, 1988).
Die American Academy of Pediatrics und der Advisory Committee on Immunization Practices empfehlen, dass OPV im Alter von 2, 4 und 15 Monaten und wieder im Alter von 4 bis 6 Jahren verwaltet werden. Wenn IPV verwendet wird, sollte es nach dem gleichen Zeitplan wie OPV gegeben werden.
2 Biologische Ereignisse nach der Immunisierung
Jeder der drei immunologisch verschiedenen Arten von Poliovirus-Typen 1, 2 und 3 kann eine paralytische Erkrankung verursachen. Sowohl IPV als auch OPV stimulieren Immunantworten gegen alle drei Virusarten. OPV induziert Magen-Darm-Schleimhaut Immunität in einem größeren Grad als IPV. Die heute in den Vereinigten Staaten verwendete Hoch-Potenz IPV erzeugt eine humorale Antikörper-Antwort, die der von OPV überlegen ist (Onorato et al., 1991). Es ist nicht klar, ob OPV oder IPV lebenslange Immunität verleiht (Nishio et al., 1984). Der Mechanismus der Abschwächung der Neurovirulenz und der der gelegentlichen Rückkehr zur Neurovirulenz wurde in einer kürzlich erschienenen Rezension ausführlich beschrieben (Racaniello, 1992). Die Empfänger von OPV verbreiten das Virus in ihren Kot, und Kontakte, die dem Virus ausgesetzt sind, können sich infizieren.
3 Poliomyelitis
3.1 Klinische Beschreibung
Die Infektion mit dem Poliovirus kann mehrere Formen annehmen:
Etwa 4 bis 8 Prozent aller Wildtyp-Poliovirus-Infektionen führen zu einer nichtparalytischen Poliokrankheit. Dies manifestiert sich als Fieber, Unwohlsein, Kopfschmerzen, Übelkeit, Steifheit von Hals und Rücken und Hirnhaut-Anzeichen. Etwa 1 Prozent der Infektionen führen zu einer paralytischen Erkrankung. Bei der paralytischen Poliomyelitis dringt das Virus in das zentrale Nervensystem ein und repliziert in motorischen Neuronen im vorderen Horn des Rückenmarks, im Hirnstamm und im motorischen Kortex. Wenn die Virusreplikation eine ausreichende Anzahl von Neuronen zerstört, findet eine Lähmung statt (Racaniello, 1992). Die Krankheit beginnt mit Kopfschmerzen, Fieber und steifem Hals; Darauf folgt eine Lähmung der bewussten Muskeln, die zuvor von den zerstörten Neuronen des Rückenmarks oder des Hirnstamms kontrolliert wurden. Die Muskellähmung ist meist asymmetrisch. Die Spinalflüssigkeit enthält eine erhöhte Anzahl von Lymphozyten, die Proteinkonzentration ist erhöht und die Glukosekonzentration normal.
3.2 Geschichte des vermuteten Zusammenhangs
Die Verbindung zwischen lebendem abgeschwächtem Polio-Impfstoff und Fällen von paralytischer Poliomyelitis geht zurück auf die Zeit der Verabreichung des ersten lebenden abgeschwächten Polio-Impfstoffs, der von Kolmer in den 1930er Jahren ausprobiert wurde (Kolmer, 1936). Leake (1935) beschrieb neun Fälle von Poliomyelitis, die nach der Impfung mit dem Kolmer-Impfstoff auftraten, und das schien durch den Impfstoff verursacht zu werden. Das Konzept, dass lebender abgeschwächter Polio-Impfstoff eine kleine Anzahl von Poliomyelitis Fällen bewirkt, hat also eine Geschichte von mindestens sechs Jahrzehnten.
Kurz nach der Lizenzierung von Sabin's OPV berichtete das United States Communicable Diseases Center ...
(CDC, später das Center for Disease Control, die Centers for Disease Control und in jüngster Zeit die Zentren für die Krankheitskontrolle und Prävention)
... die Beobachtung von Impfstoff-assoziierten Fällen von paralytischer Polio. Henderson et al. (1964) fassten Daten für die Vereinigten Staaten zusammen, die von der CDC 1962, 1963 und 1964 gesammelt wurden. Sie bewerteten 123 Fälle von paralytischen Polio, die innerhalb von 30 Tagen nach der OPV-Verabreichung aufgetreten waren, und beschlossen, dass 57 Fälle mit einer Impfstoff-induzierten Krankheit kompatibel waren.
Nach der Veröffentlichung der Arbeit von Henderson et al. (1964) erschienen weitere Fallberichte, die die Impfstoff-assoziierte paralytische Polio bei Empfängern und Kontakten der Empfänger dokumentieren. Tabelle 7-1 fasst die frühen Fallberichte zusammen, die die Impfstoff-assoziierte Poliomyelitis beschrieben haben.
 |
TABELLE 7-1: Frühe Reports über Impfung-assoziierte Poliomyelitis, erschienen vor 1970. |
3.3 Nachweis des Zusammenhangs
3.3.1 Biologische Plausibilität
OPV besteht aus lebenden attenuierten Viren, die sich im Darmtrakt vermehren und die zu einer virulenteren Form zurückkehren kann, was zur Erkrankung führt. Ein Impfstoffempfänger scheidet Lebendviren über mehrere Wochen, und Empfänger oder Kontakte können mit dem Virus infiziert werden.
3.3.2 Fallberichte, Fallserien und unkontrollierte Beobachtungssstudien
Seit den 1960er Jahren gab es etwa 100 Studien, in denen einzelne Fälle, Fallreihen und nationale Überwachungen von Impfstoff-assoziierten Fällen paralytischer Poliomyelitis berichtet wurden. Falldefinitionen wurden von der CDC und der Weltgesundheitsorganisation (WHO) gut entwickelt; Ein Fall von Impfstoff-assoziierter paralytischen Poliomyelitis wird bei Empfängern auftreten, wenn die Krankheit 7-30 Tage nach der Impfung einsetzt und bei Personen im Kontakt mit Impfstoff-Empfängern, wenn die Krankheit 7-60 Tage nach der Empfänger-Impfung einsetzt. Labortests können den Stamm des infizierenden Virus als Wildtyp- oder Impfstoffstamm des Poliovirus identifizieren. Die oben beschriebenen Fälle im Abschnitt "Geschichte des vermuteten Zusammenhangs" sind typisch für diejenigen, die in den 1970er und 1980er Jahren folgten.
WHO und CDC haben seit fast 30 Jahren Standarddefinitionen von Fällen paralytischer Poliomyelitis verwendet und viele Nationen haben Polioüberwachungssysteme zur Überwachung ihrer Polio-Immunisierungsprogramme eingeführt. Tabelle 7-2 fasst nationale Daten aus den Vereinigten Staaten, England und Wales, Belgien, Spanien, Rumänien, Ungarn, Italien und Nordgriechenland zusammen. Trotz der Unterschiede in der Art und Weise, wie Daten kategorisiert und gemeldet werden, und die Veränderungen in der Inzidenz von Polio von 1959 bis zur Gegenwart, zeigen alle nationalen Daten eine geringe Inzidenz von Impfstoff-assoziierter paralytischer Polio, in der Größenordnung von einigen Fällen pro 1 Million Dosen gegeben oder ein paar Fälle pro 1 Million Impfstoffempfänger. Die CDC-Daten für die Jahre 1975 bis 1984 zeigen eine Inzidenz von 1 Fall von Impfstoff-assoziierten paralytischen Polio pro 3,22 Millionen Dosen OPV (Centers for Disease Control, 1986, Nkowane et al., 1987). Wenn man Fälle von abwehrschwachen Empfängern und Kontakten und Patienten mit Impfstoff-ähnlichen Viren einschließt, ist die Inzidenz 1 Fall pro 2,64 Millionen Dosen OPV (Centers for Disease Control, 1986, Nkowane et al., 1987). Die Inzidenz ist mit der ersten Impfstoffdosis größer. Die CDC hat geschätzt, dass die Gesamtdosis-bezogene Inzidenz 1 Fall pro 520.000 ersten Dosen ist, im Vergleich zu 1 Fall pro 12,3 Millionen nachfolgender Dosen (Nkowane et al., 1987).
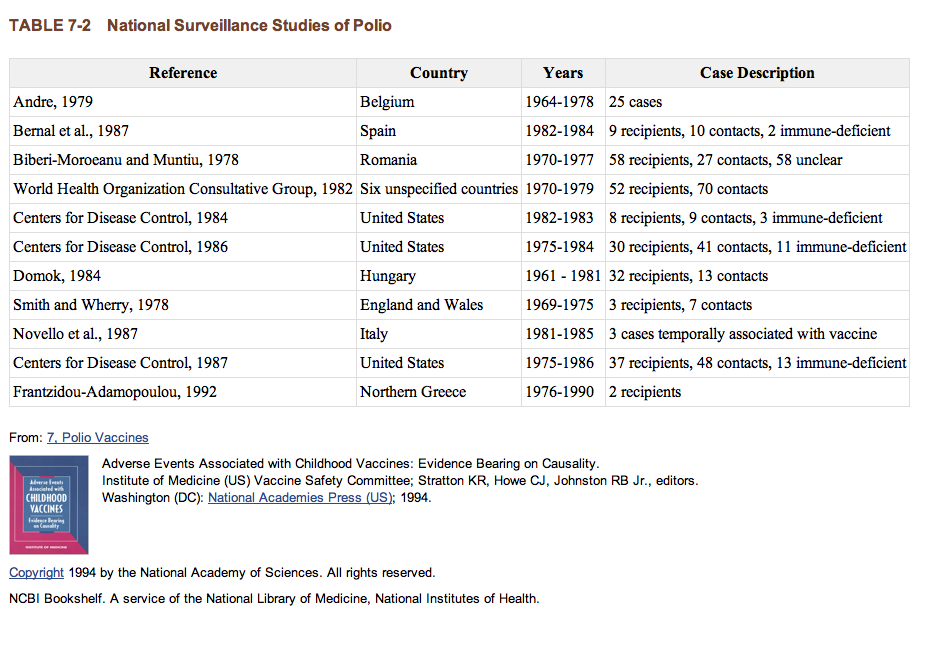 |
TABELLE 7-2: Nationale Polio-Übersichtsstudien. |
Das Monitoring System für Nebenwirkungen nach der Immunisierung (MSAEFI) führt keine Poliomyelitis als separates unerwünschtes Ereignis auf, obwohl es unter Kategorien wie "andere neurologische Symptome", "andere Reaktionen" und "ernsthafte Ereignisse" eingeschlossen werden könnte. "Das Impfstoff Adverse Event Reporting System" (VAERS) enthält mehrere Berichte (eingereicht zwischen November 1990 und Juli 1992), die Fälle von Poliomyelitis sein können, aber die Daten sind in der Regel nicht ausreichend, um festzustellen, ob ein Fall von Impfstoff-assoziierten Polio aufgetreten ist. Von den acht VAERS-Berichten, die eine Impfstoff-assoziierte Poliomyelitis nahelegten,
Die Daten über die OPV-bezogene nichtparalytische Polio sind knapper als die für die paralytische Erkrankung. Ein Bericht über die Poliomyelitisüberwachung in England und Wales von 1969 bis 1975 dokumentierte 44 Fälle von nichtparalytischer Poliomyelitis (Smith und Wherry, 1978). (Einbezogen in diese Definition wurden Patienten mit einer klinischen Diagnose "nichtparalytische Poliomyelitis" sowie Patienten mit Enzephalitis oder aseptischer Meningitis, bei denen durch Kultur oder Serologie eine Poliovirusinfektion belegt wurde). 12 dieser Fälle-vermutet man- sind mit der Verabreichung von OPV assoziiert (11 bei den Empfängern, 1 in einem Kontakt). Poliovirus wurde aus 8 der 11 Empfänger-Fälle isoliert. Bei allen Viren wurde mit dem Reproduktionskapazitätstemperatur-Test (RCT) festgestellt, dass sie vom Typ des Impfstamms sind. Das Virus, das von dem einen Kontaktfall isoliert wurde, wurde ebenso auf den Impfstamm zurückgeführt.
Die Autoren berechneten Inzidenzraten von 0,1 pro 1 Million Einwohner pro Jahr für die paralytischen und nichtparalytischen Krankheitsformen.
Die Autoren stellten fest, dass die Definition der nichtparalytischen Erkrankung vielleicht breitgefasst war und somit dies eine Schätzung der höchstmöglichen Anzahl von nichtparalytischen Fällen darstellt.
Poliovirus wurde von vor kurzem geimpften Patienten im ehemaligen Westdeutschland zwischen 1965 und 1970 (Thraenhart und Kuwert, 1972) isoliert. Von den 34 Patienten mit aseptischer Meningitis wurde das von 17 Patienten isolierte Virus vom RCT-Test als Impfstamm zugehörig, von 13 Patienten als Wildtyp und von 4 Patienten als Zwischenprodukt charakterisiert. Eine Studie über die Inzidenz von aseptischer Meningitis in Olmsted County, Minnesota, von 1950 bis 1981, berichtete, dass 2 der 283 Patienten mit aseptischer Meningitis Polio-Impfstoff innerhalb von 4 Wochen vor Beginn der Symptome erhalten hatten (Beghi et al., 1984). Allerdings wurde Virusisolation nicht berichtet, und die Krankheit kann daher dem Impfstoff nicht zugeschrieben werden.
3.3.3 Kontrollierte Beobachtungsstudien
Keine.
3.3.4 Kontrollierte klinische Studien
Keine.
3.4 Kausalitätsargument
Die Impfung mit lebenden Viren imitiert einen natürlichen Prozess der Viren-Exposition, die zu einer Immunität gegen die Krankheit führt. Obwohl das Impfstoffvirus abgeschwächt ist, führt etwa 1 in 1 Million Impfungen mit abgeschwächtem Virus zu einer paralytischen Erkrankung. Die Infektion im Darmtrakt mit dem Impfstamm des Poliovirus führt zu einer Virusausscheidung mit dem Kot und der Gefahr, dass die Kontakte eines Geimpften infiziert werden. Das Impfstoffvirus kann sich in eine virulente Form zurückverwandeln, und dies demonstriert biologische Plausibilität für die Feststellung, dass gelegentliche Kontakte von Impfstoffempfängern sich Polio zuziehen.
Eine paralytische Poliomyelitis, als unerwünschtes Ereignis, das mit der OPV-Impfung einhergeht, tritt bei OPV-Empfängern und Kontakten von OPV-Empfängern auf. Die Anwesenheit von Impfstoffvirus bei Patienten, die im Verdacht stehen, eine Impfstoff-assoziierte Polio zu haben, wird oft durch Labortests bestätigt, die eine spezifische Identifizierung des Virus als Impfstoff oder Wildtyp-Virus ermöglichen. In Ländern, in denen Wildtyp-Poliovirus fast ausgelöscht wurde, gibt es normalerweise kein anderes Mittel zur Exposition gegenüber Poliovirus, das einen Fall von Polio erklären könnte. Die Bestätigung durch Labortests, die Abwesenheit von zirkulierendem Wildtyp-Virus und die zeitliche Assoziation der paralytischen Polio mit dem Erhalt von OPV (Beginn der Erkrankung innerhalb von 30 Tagen nach der Exposition bei Empfängern und 60 Tagen bei Kontakten von Impfstoffempfängern), die alle in den gut dokumentierten Fällen von Impfstoff-assoziierten Polio gesehen wurden, erfüllen die Kriterien der Infektionskrankheit Kausalität. Die Überwachung der nichtparalytischen Polio nach der OPV-Verabreichung war viel weniger rigoros und damit weniger gut dokumentiert in der Literatur. Die Argumente zur Unterstützung der Kausalbeziehung zwischen OPV und paralytischer Poliomyelitis gelten ganz sicher für die Beziehung zwischen OPV und nichtparalytischer Polio. Der quantitative Beweis ist jedoch weniger vollständig.
3.5 Schlussfolgerung
Die Faktenlage stellt eine Kausalbeziehung zwischen OPV und paralytischer und nichtparalytischer Polio dar. Die Inzidenz der paralytischen Polio in OPV-Empfängern wurde gut dokumentiert und ist mit der ersten Impfdosis größer. Die CDC hat geschätzt, dass die Gesamtdosis-bezogene Inzidenz der paralytischen Erkrankung 1 Fall pro 520.000 ersten Dosen ist, im Vergleich zu 1 Fall pro 12,3 Millionen nachfolgende Dosen (Nkowane et al., 1987). Es ist klar, dass OPV auch bei Kontakten zu einer Impfstoff-Infektion führen kann. Es gibt keine Daten, mit denen eine Inzidenz berechnet werden kann, aber auf der Grundlage von Daten über die Wildtyp-Poliovirus-Infektion wird erwartet, dass die Inzidenz von Impfstoff-bezogenen nichtparalytischen Erkrankungen etwas größer als die Inzidenz von paralytischen Erkrankungen ist.
3.6 Risiko-modifizierende Faktoren
Der Immunzustand eines Impfstoffempfängers oder eines Kontakts eines Impfstoffempfängers verändert das Risiko der Polio als Nebenwirkung, die mit der OPV-Impfung einhergeht. Unter den OPV-Empfängern werden oft verschiedene Arten von Immunschwäche diagnostiziert, wenn ein Patient nach der Immunisierung mit OPV Polio entwickelt hat. Diese Fälle sind in Tabelle 7-3 beschrieben. Nicht-immune Kontakte haben ein erhöhtes Risiko für die Entwicklung von Polio, nachdem sie einer mit OPV immunisierten Person ausgesetzt waren. Diese Fälle sind in Tabelle 7-4 beschrieben.
Die meisten Fallberichte beschreiben nichtimmunisierte Kontakte, die sich Polio zugezogen haben, aber zwei Fallberichte beschreiben immunschwache Kontakte, die sich Polio zugezogen haben. Sowohl bei den Impfstoffempfängern als auch bei ihren Kontakten können Fallberichte repräsentativ sein für die mit der Impfung einhergehenden Fälle von Polio bei immungeschwächten Personen. Die CDC berichtet über Fälle von Polio unter immungeschwächten Menschen, ohne den Fall als Kontakte oder Empfänger zu kategorisieren (Centers for Disease Control, 1984, 1986). Nicht-immunisierte Geschwister und Spielkameraden der Empfänger sind weithin gefährdet, sich Polio zuzuziehen und können eine besondere Risikogruppe darstellen. Mit dem zunehmend jüngeren Alter des Einstiegs in die Tagespflege gibt es eine wachsende Gruppe von nicht-immunisierten Säuglingen, die Kindern, die vor kurzem mit OPV immunisiert wurden, ausgesetzt sein können. Eine Überprüfung durch den Ausschuss enthüllte Fallberichte von zwei Säuglingen im Alter von 20 Tagen und 4 Monaten (Bergeisen et al., 1986, Wilson und Robinson, 1974), die nicht immunisiert waren und die sich Polio durch dem Kontakt mit einem Pfleger und anderen Säuglingen zuzogen.
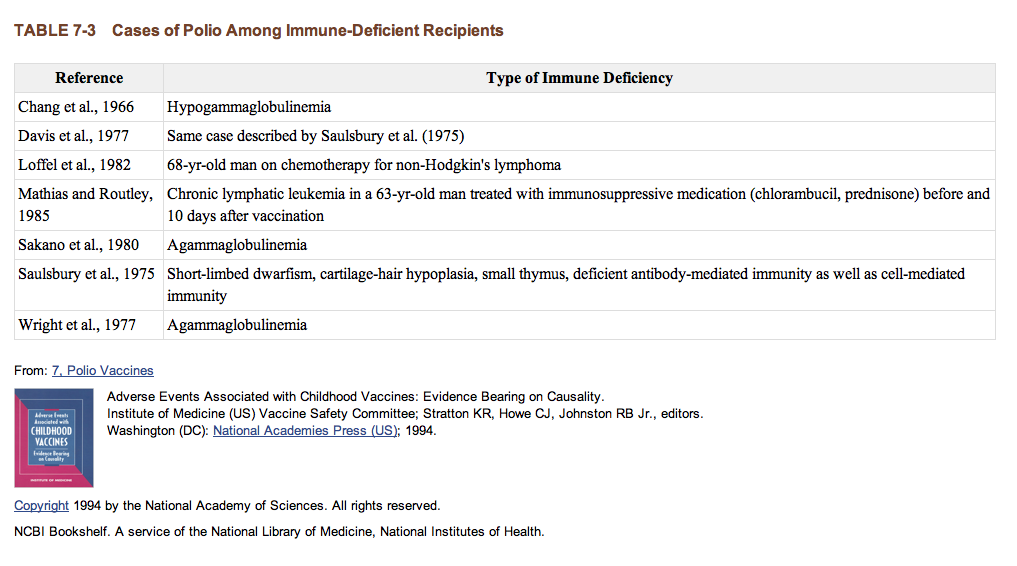 |
TABELLE 7-3 Fälle von Polio unter immungeschwächten Empfängern. |
 |
TABELLE 7-4 Fälle von Polio unter nicht-immunen Kontakten von Polio-Empfängern. |
4 Transversale Myelitis (Muskelinfektion)
4.1 Klinische Beschreibung
Transversale Myelitis ist durch den akuten Beginn von Anzeichen von Rückenmarkserkrankung gekennzeichnet, die in der Regel die absteigenden motorischen Trakte und die aufsteigenden sensorischen Fasern betreffen, was auf eine Läsion (Verletzung) auf einer Ebene des Rückenmarks hindeutet. Die jährliche Inzidenz (Das jährliche Auftreten) der transversalen Myelitis in Rochester, Minnesota, von 1970 bis 1981 betrug 0,83 pro 100.000 Menschen (Beghi et al., 1982). Kapitel 3 enthält eine ausführlichere Diskussion der transversalen Myelitis.
4.2 Geschichte der vermuteten Assoziation
Es gibt keine besondere Geschichte einer Assoziation zwischen transversaler Myelitis und Polio-Impfstoffen.
4.3 Nachweis von Assoziation
4.3.1 Biologische Plausibilität
Kapitel 3 enthält eine Diskussion über die biologische Plausibilität für eine kausale Beziehung zwischen demyelinisierenden Störungen und Impfstoffen im Allgemeinen.
4.3.2 Case Reports, Case Series und nicht-kontrollierte Observationsstudien
Tabelle 7-5 fasst die drei Fälle von transversaler Myelitis zusammen, die in der Literatur nach der Impfung mit OPV nachgewiesen wurden.
Bei Säuglingen traten zwei Fälle auf.
(1) Ein siebenmonatiges Mädchen entwickelte Symptome 6 Tage nach dem Erhalt von OPV, Diphtherie und Tetanustoxoiden (DT) (Whittle und Roberton, 1977).
(2) Ein 20-monatiges Mädchen entwickelte Symptome 1 Monat nach Erhalt von OPV, Diphtherie, Tetanustoxoide und Pertussis-Impfstoff (DPT). Bei ihr wurde Hypogammaglobulinämie gefunden (Douglas und Anolik, 1981).
(3) Der dritte Fall trat bei einer 24-jährigen Frau auf, die gleichzeitig mit OPV, Typhus und Cholera-Impfstoffen geimpft wurde (D'Costa et al., 1990). Die Frau hatte zum Zeitpunkt der Impfung Fieber und hatte eine Infektion der oberen Atemwege und Pharyngitis in den 5 Wochen vor der Impfung.
Der Ausschuss kennt einen Fall von transversaler Myelitis bei einem Kind mit schwerem kombiniertem Immunschwäche-Syndrom (Richard B. Johnston, Yale University, New Haven, persönliche Kommunikation, 1993). Das Impfstamm-Poliovirus wurde aus dem Myokard isoliert.
Die VAERS haben zwei Fälle der transversalen Myelitis (eingereicht zwischen November 1990 und Juli 1992), die bei Patienten nach einer Kombination von DPT, OPV und Haemophilus influenzae Typ b (Hib) Impfstoff und einer Kombination von DPT, OPV, Masern-Mumps- Röteln-Impfstoff (MMR) und Hib-Impfstoff. Aber die zeitlichen und klinischen Details sind nicht ausreichend für eine korrekte Bewertung.
Ein weiterer VAERS-Bericht über die transversale Myelitis war ein Duplikat des im Jahr 1990 veröffentlichten Fallberichtes, der oben diskutiert wurde (die 24-jährige Frau).
Darüber hinaus hörte das Komitee auf einer öffentlichen Sitzung im Januar 1993 von einem 4-Monate alten Mädchen, das transversale Myelitis entwickelte, diagnostiziert von einem Neurologen, ein paar Tage nach ihren zweiten DPT und OPV Immunisierungen. Die das Mädchen behandelnden Ärzte nahmen an, dass ein Zusammenhang mit ihren Impfungen besteht (siehe Anhang B).
Berichte, die transversale Myelitis mit Polio-Impfstoff assoziieren.
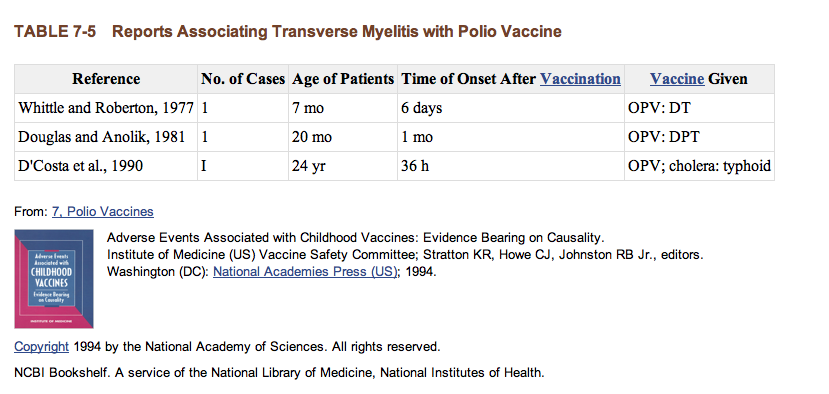 |
Tabelle 7-5: Reports Associating Transverse Myelitis with Polio Vaccine. |
4.3.3 Kontrollierte Beobachtungsstudien
Keine.
4.3.4 Kontrollierte klinische Studien
Keine.
4.4 Kausalitätsargument
Es gibt biologische Plausibilität, dass virale Impfstoffe Demyelinisierungsstörungen verursachen können. Vaccine-strain Poliovirus kann in das zentrale Nervensystem eindringen und wurde mit einer peripheren Nerven-Demyelinisierungsstörung, Guillain-Barré-Syndrom (siehe nächster Abschnitt) assoziiert. Die drei Fälle von transversaler Myelitis nach dem Erhalt von OPV, die in der Literatur berichtet werden, die beiden Fälle, die in VAERS berichtet werden, und der Fall, die durch den Ausschuss in einer persönlichen Kommunikation identifiziert wurden, sind unzureichend, um eine Assoziation zwischen OPV und transversale Myelitis anzuzeigen, die über einen reinen Zufall hinausgehen. Mindestens fünf der Fälle traten nach mehreren Immunisierungen auf, was eine Beurteilung eines kausalen Zusammenhangs zwischen OPV und transversaler Myelitis erschwert. Es wurden keine Fälle von transversaler Myelitis nach dem Erhalt von IPV gemeldet.
4.5 Schlussfolgerung
Der Tatbestand ist unzureichend, um eine Kausalbeziehung zwischen OPV und transversaler Myelitis zu akzeptieren oder abzulehnen. Es gibt keine Beweise für eine kausale Beziehung zwischen Guillain-Barré-Syndrom IPV und transversale Myelitis.
5 Guillain-Barré Syndrom
5.1 Klinische Beschreibung
Guillain-Barré-Syndrom (GBS) zeichnet sich durch den schnellen Beginn von schlaffer motorischen Schwäche mit Depression von Sehnenreflexen und entzündlicher Demyelinisierung von peripheren Nerven aus. Die jährliche Inzidenz von GBS scheint etwa 1 pro 100.000 für Erwachsene zu sein. Die Daten sind nicht endgültig, aber die jährliche Inzidenz von GBS bei Kindern unter 5 Jahren scheint ungefähr gleich zu sein. Die jährliche Inzidenz von GBS bei Kindern über 5 Jahre und Jugendliche scheint niedriger zu sein. Kapitel 3 enthält eine ausführliche Diskussion über GBS.
5.2 Geschichte der vermuteten Assoziation
Eine Beziehung zwischen abgeschwächten Virusimpfstoffen und demyelinisierender Erkrankung wurde seit vielen Jahren untersucht, wie in Kapitel 3 beschrieben. Besonderes Interesse an der Beziehung zwischen GBS und Polio-Impfstoff wurde durch einen Bericht im Jahr 1976 von 10 Fällen von GBS bei Patienten, die ( Andersen und Eeg-Olofsson, 1976).
5.3 Nachweis für Assoziation
5.3.1 Biologische Plausibilität
Kapitel 3 enthält eine ausführliche Erörterung der Argumente, dass Impfstoffe eine Demyelinisierung verursachen können, einschließlich GBS. Es gibt keine zusätzlichen Daten, die die biologische Plausibilität einer spezifischen Beziehung zwischen Polio-Impfstoffen und GBS zeigen.
5.3.2 Fallberichte, Fallserien und unkontrollierte Beobachtungsstudien (Observationsstudien)
Grose und Spigland (1976) beschreiben ein 10 Monate altes Mädchen, das GBS 4 bis 7 Tage nach dem Erhalt von Masern-Impfstoff, DPT und OPV entwickelt hat. Poliovirus Typ 1 wurde aus einem Rachenabstrich isoliert. Die Autoren schrieben die Krankheit dem Masernimpfstoff zu.
Leneman (1966) prüfte die Literatur vor 1966 und beschrieb 1100 Fallberichte von GBS, die zwischen 1949 und 1966 veröffentlicht wurden. In fünf Fällen wurde die Impfung mit IPV erwähnt, obwohl das Zeitintervall zwischen der Impfung und dem Beginn der GBS nicht beschrieben wurde. Änderungen der diagnostischen Verfahren seit 1949 könnten auch einige der in dieser Zusammenfassung enthaltenen Fälle disqualifizieren. Diese Secondhand-Zusammenfassung der Fallberichte liefert keine ausreichenden Informationen, um festzustellen, ob IPV mit GBS verknüpft ist.
In einer Studie in Schweden, die ausschließlich IPV nutzte, diskutierten Andersen und Eeg-Olofsson (1976) 10 Fälle von GBS, die 1971 bei Personen unter 60 Jahren auftraten. In neun der Einzelpersonen trat der Beginn der GBS mehr als 1 Jahr nach einer Impfung mit IPV auf. Die Autoren folgerten, dass es keine Assoziation zwischen IPV und GBS gab.
Daten aus dem MSAEFI nannten 14 Fälle von GBS nach OPV-Gabe von 1979 bis 1990. In den meisten Fällen wurde OPV in Kombination mit DPT oder MMR oder beidem gegeben. VAERS hat zwei Fälle von GBS (eingereicht zwischen November 1990 und Juli 1992) nach der Verabreichung von OPV in Kombination mit DPT und entweder MMR oder Hib-Impfstoff.
5.3.3 Kontrollierte Beobachtungsstudien
Zwei kontrollierte Studien untersuchten die Assoziation zwischen GBS und Polio-Impfstoff (Tabelle 7-6).
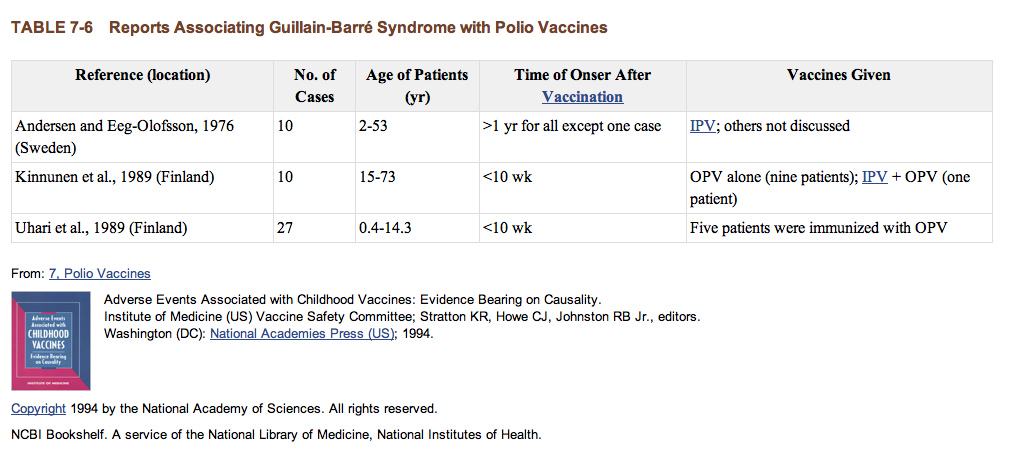 |
TABELLE 7-6 Berichte, die Guillain-Barré-Syndrom mit Polio-Impfstoffen assoziieren. |
Die erste Studie fand in einer südlichen Provinz Finnlands (Uusimaa) statt, wo die fortlaufende Überwachung von GBS von 1981 bis 1986 eine Zunahme der Inzidenz von GBS nach einem landesweiten Programm zur Immunisierung von Kindern und Erwachsenen gegen Polio aufdeckte (Kinnunen et al., 1989. ). Damals nutzte Finnland in der Regel IPV, aber ein Ausbruch von 10 Fällen von Poliomyelitis zwischen August 1984 und Januar 1985 führte zu der Entscheidung, eine Massenimpfung mit OPV durchzuführen. 54 % der finnischen Bevölkerung wurden mit OPV während eines 5-wöchigen Zeitraums zwischen dem 10. Februar und 15. März 1985 geimpft. Während und kurz nach der Impfkampagne erhelten Krankenhäuser in der südlichen Provinz Uusimaa (Bevölkerung etwa 1,17 Millionen) eine unerwartet hohe Anzahl von Patienten mit GBS. Das erste und zweite Quartal 1985 zeigten eine statistisch signifikant höhere Anzahl von Fällen von GBS, als in den anderen Quartalen der Beobachtungsperiode gefunden wurden. Im Laufe des 6-Jahres-Zeitraums von 1981 bis 1986 (einschließlich des Zeitraums der OPV-Immunisierung) war die durchschnittliche Anzahl der Fälle von GBS pro Quartal 3, und Kinnunen schätzte eine grobe jährliche Inzidenz von 1 Fall pro 100.000 Einwohner. Dies ist deutlich höher als der Mittelwert für den Zeitraum von 6 Jahren. 10 Fälle traten im ersten Quartal auf und 6 Fälle traten im zweiten Quartal 1985 auf in Zeiten, die der Immunisierungskampagne entsprechen. Zehn Patienten wurden mit GBS innerhalb von 10 Wochen nach der Impfung mit OPV diagnostiziert, wobei die mittlere Zeit des Beginns bei 31 Tagen nach der Impfung liegt. Sechs der Fälle traten innerhalb von 6 Wochen nach der Impfung auf. Alle Patienten mit vermutetem GBS wurden separat von zwei Neurologen ausgewertet, und in jedem Fall wurde ein Konsens über die Diagnose erreicht. Das Alter der Patienten reichte von 15 bis 73 Jahren.
Die Studie in Finnland nutzte zwei einzigartige Phänomene: (1) eine fortlaufende Überwachung von GBS, die Fälle in der Bevölkerung über einen Zeitraum von 6 Jahren identifizierte und (2) ein nationales Programm zur Immunisierung von Erwachsenen in einem Zeitraum von 5 Wochen. Die Daten zeigten eine Zunahme der Anzahl der Fälle von GBS, die zeitlich mit dem Immunisierungsprogramm assoziiert waren, und die Zunahme war statistisch signifikant. Die Diagnose von GBS wurde getroffen auf Grund der Verwendung von konsistenten Kriterien während des Beobachtungszeitraums wegen der prospektiven Studie über GBS, die bereits vorhanden war, und zwar gut bevor die Polio-Epidemie und Immunisierung gegen Polio geschahen.
Die Studie in Finnland zeigt, dass OPV mit GBS assoziiert werden kann und stellt die Frage auf, warum es keine anderen Berichte von GBS - OPV Verbindungen gibt. Eine Erklärung kann sein, dass die Seltenheit von GBS, die übliche Vorherrschaft von GBS bei Erwachsenen und die Seltenheit der Impfung mit OPV bei Erwachsenen keine anerkannten Fälle von OPV-assoziierten GBS produziert haben. Kinnunen et al. (1989) schätzte eine grobe jährliche Inzidenz von 1 Fall GBS pro 100.000 Bevölkerung. Die 10 Fälle, die mit Impfstoff assoziiert wurden, traten bei Patienten im Alter von 15 bis 73 Jahren auf. 6 der Patienten waren in ihren 50ern und 2 waren in ihren 30s. Wenn GBS hauptsächlich bei Erwachsenen auftritt und relativ wenige Erwachsene OPV erhalten, ist die Wahrscheinlichkeit gering, einen Fall von OPV-assoziiertem GBS ohne Überwachungssystem zu entdecken.
Zur gleichen Zeit, als Kinnunen et al. (1989) die Ergebnisse ihrer Studie veröffentlichten, publizierte Uhari et al. (1989) einen Brief, der einen Cluster von GBS-Fällen bei Kindern in Finnland beschreibt. Sie identifizierten 27 Fälle von GBS bei Kindern im Alter von 0,4 bis 14,3 Jahren über den Zeitraum von 7 Jahren von 1980 bis 1986 mit einer durchschnittlichen Inzidenz von 3,9 Fällen pro Jahr. Sie bemerkten auch einen Höchststand von 10 Fällen im Jahr 1985, der sich von der Anzahl der Fälle unterscheidet, die in anderen Jahren festgestellt wurden, und der Unterschied war statistisch signifikant (P = 0,0042). Im Gegensatz zu Kinnunen et al. (1989) bestätigten Uhari und Kollegen nicht, dass die Kinder mit GBS innerhalb von 6 Wochen vor dem Beginn der GBS tatsächlich OPV erhalten hatten. Sie demonstrierten eine ökologische und zeitliche Assoziation zwischen der OPV-Kampagne und dem Cluster von GBS-Fällen.
5.3.4 Kontrollierte klinische Versuche
Keine
5.4 Kausalitätsargument
Andere Viren und Impfstoffe wurden mit GBS assoziiert (siehe Kapitel 3), und es ist biologisch plausibel, dass OPV auch mit GBS assoziiert sein kann. Von den beiden kontrollierten Studien, die die Beziehung zwischen OPV und GBS untersuchen, zeigte eine Studie den Nachweis, dass es bei Erwachsenen eine Wirkung geben kann, und die zweite Studie schlug vor, dass es bei Kindern eine Wirkung geben kann (Tabelle 7-6). Das Fehlen anderer Berichte steht im Einklang mit der geringen Inzidenz von GBS (grob geschätzt handelt es sich um eine jährliche Inzidenzrate von 1 Fall pro 100.000 Menschen). Die Beobachtung einer erhöhten Inzidenz von GBS in Finnland, die zeitlich mit einer Massenimpfung mit OPV verbunden war, stellte eine besondere Gelegenheit dar, die Assoziation zwischen GBS und OPV zu studieren. Die Konsistenz der diagnostischen Kriterien und statistisch signifikanten Unterschiede in der Inzidenz von GBS deuten darauf hin, dass die Zunahme nicht auf Zufallsvariation oder voreingenommene Fallberichterstattung zurückzuführen war.
Der Ausschuss schätzte relative Risiken und Risikounterschiede für GBS nach OPV auf der Grundlage der Studien von Kinnunen et al. (1989) und Uhari et al. (1989). Die erwartete Anzahl von Fällen wurde berechnet, indem man aus den Hintergrund-Inzidenzdaten die Zeitspanne eliminiert hat, in der OPV gegeben wurde (die die Autoren in ihren Berechnungen nicht gemacht haben). Dies führte zu relativen Risiko- (RR) Schätzungen von 3,8 für die Studie von Kinnunen et al. (1989) und 3.6 für die Studie von Uhari et al. (1989). Die Risikodifferenz ... (berechnet als [RR - 1] x Hintergrundinzidenz) ... für GBS bei Erwachsenen auf der Grundlage der relativen Risiko- und Hintergrundinzidenz, die von Kinnunen et al. Ist 2,5 pro 100.000 pro Jahr. Da OPV-induzierte GBS innerhalb von 6 Wochen nach der Impfung auftritt, ist das 6-Wochen-Überschussrisiko 0,3 pro 100.000. Durch die Verwendung der Hintergrundraten und relativen Risiken von Uhari et al. beträgt die Risikodifferenz für GBS innerhalb von 6 Wochen nach OPV bei Kindern unter 15 Jahren etwa 0,1 pro 100.000.
Demgegenüber deuten die von Winner und Evans (1990) und Hankey (1987) bereitgestellten Daten jedoch darauf hin, dass die Inzidenzrate für Kinder mit der Altersstufe variiert. Basierend auf den letzteren Daten könnte die Risikodifferenz bei kleinen Kindern signifikant größer sein als die, die auf der von Uhari et al beschriebenen Hintergrund-Inzidenz basiert, und sie könnte sich der bei Erwachsenen nähern. Relativ wenige Erwachsene in den Vereinigten Staaten erhalten OPV. So wäre der Anteil der GBS-Fälle bei Erwachsenen, die auf OPV zurückzuführen sind, klein.
5.5 Schlussfolgerung
Die Sachlage begünstigt die Annahme eines Kausalzusammenhangs zwischen OPV und GBS. Das relative Risiko auf der Grundlage von Studien in Finnland ist in der Größenordnung von 3,5 für Erwachsene, und die Risikodifferenz beträgt etwa 2,5 pro 100.000 Menschen. Schätzungen der Hintergrund-Inzidenzraten für GBS bei Kindern variieren. Es ist nicht klar, was das relative Risiko und die Risikodifferenz für Kinder in den Vereinigten Staaten ist (siehe Kapitel 3). Die Sachlage ist unzureichend, um eine Kausalbeziehung zwischen IPV und GBS zu akzeptieren oder abzulehnen.
5.6 Risiko-modifizierende Faktoren
GBS, als separater diskreter Angriff, tritt bei einem kleinen Prozentsatz der zuvor betroffenen, vielleicht 2 bis 3 Prozent, erneut auf ("Rezidiv"), und von einigen Personen ist bekannt, dass sie drei oder vier separate Episoden hatten. Anders als der Patient, der von Pollard und Selby (1978) beschrieben wurde, der drei Angriffe erlebt hat, sind innerhalb von 10-21 Tagen nach Erhalt des Tetanustoxoids Fälle von Rezidiven nach der Impfung nicht dokumentiert. Dennoch, wenn GBS innerhalb von 5 Tagen bis 6 Wochen nach einer Impfung auftritt, können nachfolgende Impfungen mit OPV oder verschiedenen Immunogenen mit einem größeren Risiko von GBS verbunden sein, als wenn die Person nie GBS gehabt hätte. Eine Vorgeschichte von GBS ohne Bezug auf eine Impfung ist ein noch unsicherer Risikofaktor.
6 Anaphylaxie und Thrombozytopenie
6.1 Klinische Beschreibung
Anaphylaxie ist eine plötzliche, potenziell lebensbedrohliche systemische Erkrankung, die durch hochreaktive Moleküle aus Mastzellen und Basophilen vermittelt wird. Die klinischen Manifestationen der Anaphylaxie umfassen Blässe und dann diffuses Erythem, Urtikaria und Juckreiz, subkutane Ödeme, Ödeme und Krampf des Kehlkopfes, Keuchen, Tachykardie, Hypotonie und hypovolämischer Schock, die in der Regel innerhalb von Minuten nach der intramuskulären oder subkutanen Antigen-Exposition auftreten. Im Kapitel 4 findet sich eine ausführlichere Diskussion der Anaphylaxie.
Thrombozytopenie ist eine Abnahme der Zahl der Thrombozyten, die an der Blutgerinnung beteiligt sind. Thrombozytopenie kann aus dem Scheitern der Thrombozytenproduktion, einer verkürzten Thrombozytenlebensdauer oder einer abnormen Verteilung der Blutplättchen im Körper resultieren. In den meisten Fällen ist die Thrombozytopenie bei Kindern mild und vorübergehend, und es wird oft nur zufällig entdeckt, wenn ein vollständiges Blutbild hergestellt wird. Schwere Thrombozytopenie mit spontanen Blutungen verbunden, einschließlich Blutungen in die Haut, heißt thrombozytopenische Purpura. Für keine der Zustände wurden bevölkerungsbasierte Inzidenzraten identifiziert. Der Ausschuss wurde gebeten, die Daten über eine mögliche Kausalbeziehung zwischen IPV allein und Anaphylaxie und Thrombozytopenie zu bewerten.
6.2 Nachweis für Assoziation
Es gibt keine veröffentlichten Berichte über Anaphylaxie oder thrombozytopenische Purpura, die mit IPV assoziiert ist.
6.3 Schlussfolgerung
Es gibt keine Beweise für einen ursächlichen Zusammenhang zwischen IPV und Anaphylaxie. Es gibt keine Beweise für einen ursächlichen Zusammenhang zwischen IPV und Thrombozytopenie.
7 Tod
Eine ausführliche Erörterung der Beweislage von Tod nach Immunisierung findet sich im Kapitel 10. Nur das Kausalitätsargument und die Schlussfolgerung folgen hier.
7.1 Kausalitätsargument
7.2 Schlussfolgerung
Die Evidenz stellt einen ursächlichen Zusammenhang zwischen OPV und Tod aus einer Impfstoff-Stamm-Poliovirus-Infektion dar, einschließlich einer Infektion, die zu einer paralytischen Poliomyelitis führt. Die Schlussfolgerung basiert auf Fallberichten und nicht auf kontrollierten Studien. Es kann kein relatives Risiko berechnet werden. Allerdings scheint das Risiko des Todes durch OPV-bezogenen Polio-Infektionen außerordentlich niedrig zu sein.
Die Beweislage begünstigt die Annahme eines Kausalzusammenhangs zwischen OPV und Tod durch GBS. Es gibt keinen direkten Beweis dafür. Die Schlussfolgerung beruht auf dem Potenzial von GBS, tödlich zu sein. Das Risiko scheint außerordentlich niedrig zu sein.
Die Beweise sind unzureichend, um eine kausale Beziehung zwischen Polio-Impfstoffen und SIDS zu akzeptieren oder abzulehnen. Der Beweislage ist unzureichend, um eine Kausalbeziehung zwischen OPV und Tod aus anderen Ursachen als den oben aufgeführten zu akzeptieren oder abzulehnen.
8 Literaturnachweis
Version: 8.5.2017
Adresse dieser Seite
Home
Dr. Joachim Gruber